- елементи
- абстрактно
- Въведение
- Материали и методи
- Описание на изследването
- Статистически анализ
- Анализ на мрежата
- Приписване на целия геном
- резултатът
- дискусия
- Допълнителна информация
- Word документи
- Допълнителна информация
елементи
- Биполярно разстройство
- Проучвания за асоцииране в целия геном
- Затлъстяване
абстрактно
Биполярното разстройство (BD) има висока наследственост, оценена между 60% и 85%. 1, 2 Проведени са няколко проучвания за асоцииран геном (GWA), за да се идентифицират често срещаните генетични рискови фактори за BD. Въпреки че варианти на алели са идентифицирани в различни гени, включително ANK3, CACNA1C и ODZ4, 3, 4, 5, 6, тези варианти варират в широки граници между проучванията и обясняват много ограничена част от наследяването на BD.
Смята се, че сложните фенотипове, включително психиатрични разстройства като BD, включват голям брой екологични и генетични компоненти, които взаимодействат при огнища на болести. В допълнение, те могат да споделят варианти на генетичен риск с други фенотипни белези. Следователно модели, включващи съответни фенотипни белези като ковариати и взаимодействащи рискови фактори, трябва да бъдат взети предвид, когато се търсят генетични фактори, допринасящи за сложни фенотипове.
По-специално, BD е положително свързан с много фенотипни характеристики, включително затлъстяване (обикновено се определя като индекс на телесна маса (ИТМ) 30 kg/m 2) и следователно с по-висок ИТМ, като едно проучване в напречно сечение показва степен на затлъстяване от 41 % BD в сравнение с 27% при пациенти без BD. 8 Тази коморбидност има значителни клинични последици, тъй като няколко проучвания показват, че биполярните пациенти с коморбидно затлъстяване имат по-висока психиатрична и обща тежест на заболяването и повишен рецидив на настроението. 9, 10, 11, 12 Например, открихме по-висок процент на преяждане, по-висок процент на самоубийства и по-висока обща медицинска тежест при пациенти с BD и по-висок ИТМ, 12, което предполага, че този фенотип определя клинично важна подгрупа. В допълнение, ИТМ е наследен сложен признак 13, който също е свързан с други психиатрични разстройства, включително шизофрения, голямо депресивно разстройство и прекомерен прием на храна, 14, 15 мотивиращ включването на ИТМ в изследването на генетични рискови фактори за метаболитни и психиатрични фенотипове.
Положителната връзка между BD и BMI (като мярка за затлъстяване) заедно с наследяването на BD и BMI предполага възможно взаимодействие в генетичните механизми, лежащи в основата на тези черти. Предишни проучвания на GWA за диабет тип 2 (T2D) и инсулинова резистентност показват, че отчитат разликите в BMI 16 и взаимодействията с единичен нуклеотиден полиморфизъм (SNP) -BMI 17. Причината за тези проучвания е да се включи медиираното качество на затлъстяване, измерено чрез ИТМ, в хетерогенната етиология на фенотипи като T2D и инсулинова резистентност. 18 По отношение на ефектите върху ИТМ, тези проучвания идентифицират значителни рискови места. В T2D анализи в случая на контрол на стратификацията на случая на консорциум на Wellcome Trust в зависимост от състоянието на затлъстяването, Timpson et al. 16 идентифицира вариант на TCF7L2 - известен силен ген за чувствителност към T2D - преди това не е бил идентифициран в цялата кохорта. Освен това Manning et al. изследва ефектите на SNP върху инсулин на гладно, като отчита ефекта на BMI, както и потенциалните взаимодействия SNP-BMI и наблюдава шест нови значими локуса на целия геном (P 16, 17
Въпреки известните корелации между BD и затлъстяването, BMI все още не е включен в проучванията на GWA BD. Въз основа на обосновка, подобна на тази, използвана в изследванията на T2D, ние предлагаме да се намали фенотипната хетерогенност на BD, като се вземат предвид разликите в ИТМ между пациенти с BD и здрави индивиди, както и потенциалните взаимодействия на SNP-BMI относно чувствителността към BD заболяване. Използвайки публично достъпни данни от предишно проучване на GWA, проведено от Информационната мрежа на генетичните асоциации (GAIN) 4, ние преоценяваме генетичните асоциации с BD, като същевременно включваме данни за максималната жизненост на ИТМ. По-специално, направихме анализи на GWA, адаптирани към ИТМ, и изследвахме потенциалните взаимодействия на SNP-BMI.
Материали и методи
Описание на изследването
Консорциумът за изследване на генома за биполярно разстройство (BiGS) проведе проучване на GWA върху BD; данните са на разположение като част от данните за GAIN BP в dbGaP 19 и по-рано описани от Smith et al., 4 включително описания на изследваните субекти и процедури за генотипиране и контрол на качеството. Въпреки че проучването BiGS/GAIN включваше данни от европейско-американски (EA; N = 2035) и афро-американски (AA; N = 1015) субекти, ние ограничихме нашите анализи до субекти от EA, за да избегнем стратификация на населението.
По време на 18-годишния период на набиране, 1001 субекти от BD са регистрирани в няколко институции. Всички случаи отговарят на критериите за биполярно разстройство I, както е определено от DSM IV. Въпреки това, лица, наети по различно време, бяха интервюирани с Диагностичното интервю за генетични изследвания 2, 3 или 4 (DIGS 2, 3, 4). Действителната височина (инчове) и максимално телесно тегло през целия живот (паунда) бяха събрани само в DIGS 4 и следователно отделно докладваният максимален ИТМ (максимален ИТМ) беше наличен само в подгрупа от 388 случая на ЕА. Текущо телесно тегло и други измервания на телесното тегло, различни от максималното телесно тегло през целия живот, не са били налични.
Контролните субекти попълниха отделен психиатричен въпросник и бяха изключени, ако отговаряха на диагностичните критерии за депресия или имаха анамнеза за BD или психоза. Проверките бяха сравнени със случаи по пол и етническа принадлежност. 4 Контролният въпросник събра текущата височина и максималния живот на тялото, а данни за BMI с максимална стойност на BMI бяха използвани за 1020 контрола на EA.
Статистически анализ
Както вече споменахме, анализите бяха ограничени до извадката на EA, за да се избегнат неясноти според структурата на популацията. Освен това използвахме анализ на основните компоненти като гаранция за по-нататъшно коригиране на стратификацията на популацията. 21 Оценихме четирите основни компонента (PC) и установихме, че нито един не е свързан с BD или max BMI (P> 0,5). Поради тази причина докладваните анализи не се коригират за компютър. QQ графики бяха използвани за измерване на степента на инфлация на статистиката на асоциациите и бяха извършени анализи на чувствителността, коригирани за най-високите геномни асоциации за първия компютър.
Всички анализи бяха извършени в R Statistics Software, версия 2.14.0 (//www.r-project.org/). Използвахме статистически значим праг от P 22 и целият геном беше приписан на фазирани данни, използвайки Impute 2.2.2, 23, като използвахме фазови данни за генома (всички популации) като референтен панел. SNPs с лошо качество на присвояване бяха премахнати (доза R2
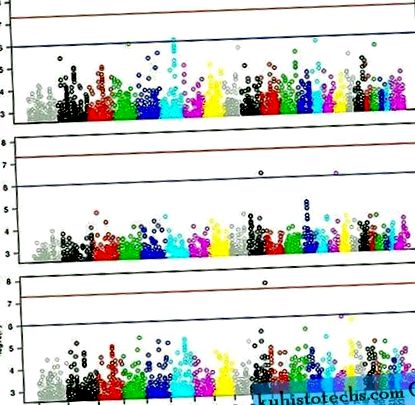
Парцели в Манхатън за анализ на GWA. За всеки SNP се нанася −log 10 (стойност P) (ос y) спрямо хромозомната позиция (ос x) за ( а ) пределен SNP ефект, коригиран за ИТМ (без взаимодействие SNP-BMI), ( б ) Ефект от взаимодействието SNP-BMI и ( ° С ) съвместен генетичен тест, отчитащ макс. ИТМ и потенциално взаимодействие SNPxBMI.
Изображение в пълен размер
- Изтеглете слайд на PowerPoint
Други сигнали за най-висока асоциация включват rs17541406 в псевдогенен SEPHS1P2, надолу по веригата от MCTP2 (P = 1, 21E-6), със същия модел на ИТМ-зависим генетичен ефект. Вариантите в кодиращите протеина региони на WW домейн оксидоредуктазата (WWOX) (rs11150078, P = 1, 73E - 6) и CDH23 (rs1625975, P = 4, 16E - 6) също бяха високо оценени и бяха доказани доказателства за взаимодействащи ефекти (Таблица) 1, снимки 1б и в).
По-малкият алел rs7690204 в GYPA кодиращия протеин регион показва пределен защитен ефект (вероятностно съотношение = 0,65, P = 1,11 E-6; Таблица 1, Фигура 1а), но без SNP-BMI взаимодействия. По същия начин двата SNPs, разположени в междугенния регион нагоре по веригата MARCKS, rs6934970 и rs17074473 (при дисбаланс на свързване), също са високо оценени (P = 7, 08E-6 и P = 8, 23E-6, съответно; Фигура 1в) в анализът маргинален генетичен ефект след корекция за ИТМ, но не показва данни за взаимодействие с ИТМ. По-конкретно, по-малкият алел rs6934970 е свързан с повишена вероятност за BD след ИТМ (коефициент на вероятност = 1,83, P = 8,5E-7; Таблица 1, Фигура 1а).
Статистиката на тестовете за асоцииране в анализите на GWA не е силно завишена (λ = 1, 04 за теста с две степени на свобода, позволяващ взаимодействие BMI-SNP), което показва, че няма значителна стратификация на популацията. След настройка за първия компютър, резултатите са само малки промени, въпреки че степента на ефектите на някои SNPs е намалена (допълнителна таблица 1). QQ графики за некоригирани и PC-модифицирани анализи са дадени в допълнителния материал (S1 и S2).
Най-високо оценените канонични пътища, базирани на IPA, включват „синаптична дългосрочна депресия“, „сигнализиране на α-протеин G“ и „синаптично дългосрочно потенциране“ (Таблица 2). Най-добрите мрежи включват молекули, участващи в растежа и развитието на клетките, както и в развитието и сигнализирането на сърдечно-съдовата система (Фигура 2).
Маса в пълен размер
ИТМ мрежа - взаимодействие между гените, участващо в риска от BD заболяване. Мрежа с най-висок резултат, включваща много гени от каноничния път „Клетъчен растеж и пролиферация, развитие и функциониране на сърдечно-съдовата система, органично развитие“ и четвъртата най-висока оценка на мрежа, включваща много гени от клетките „Клетъчно развитие, клетъчен растеж и разпространение, скелет и каноничен път на развитие "Мускулно-скелетните и функционални функции са представени заедно, за да илюстрират взаимодействието между най-добрите гени в нашия анализ. Цветът на гените показва степента на асоциация в нашите анализи: червено = най-ниска стойност на P, розово = ниска/средна стойност на P, сиво = средна стойност на P и бяло = P> 0,001. Формите показват вида на гена/молекулата ( цитокин, транспортер, киназа и др.).). Плътните линии означават преки връзки, а прекъснатите линии означават непреки връзки. Забележка: Wnt, Wnt объркан рецептор, LPR1 ко-рецептор, сигнални протеини за трансдукция на цитоплазмен сигнал и компоненти на комплекса за унищожаване на B-катенин, AXIN1 и APC бяха добавени към мрежата, за да илюстрират каноничния път Wnt нагоре по веригата CTNNB1, GSK3B и TCF7L2 гени. изброени в нашия анализ.
Изображение в пълен размер
- Изтеглете слайд на PowerPoint
Приписаните резултати бяха подобни на тези за наблюдаваните генотипове, с по-плътни пикове в най-високите оценени стойности (Допълнителна фигура S3 показва резултатите за двустепенния анализ на свободата). Когато се анализира ефектът на SNP с две степени на свобода, включително взаимодействието BMI-SNP, се наблюдава нов пик върху хромозома 3 (допълнителна таблица 2). Този връх е в междугенния регион надолу по веригата от TRIM42 и включва SNPs rs72977016, rs182827559 и rs60035994, всички от които представляват редки вариации (по-ниска честота на алели 24, 25, 26 и особено локуса на риска за T2D в проучвания, стратифициращи субекти според BMI TCF7L Т-клетъчен фактор/лимфоиден усилвател, който при транслокация на ß-катенин в ядрото активира експресията на целеви гени надолу по веригата от каноничния път Wnt/ß-катенин.27, 28 Тази каскада на трансдукция на сигнала е свързана с много заболявания - особено рак - и участва критично в развитието на много организми, включително хората
Каноничният път Wnt/β-катенин е критичен за различни аспекти на невропластичността 30 и неврогенезата за възрастни. 31, 32, 33 Действието на стабилизаторите на настроението върху този сигнален път се счита за косвено доказателство за участието му в патофизиологията на BD. Например, антидепресантните ефекти на лития върху поведението се смятат за вторични спрямо инхибирането на β-катениновия инактиватор GSK-3β 35, 36 чрез директни 37, 38 и индиректни механизми 39; Β-катенинът има сходни ефекти с лития при модели на гризачи. Предполага се също така, че валпроатът инхибира GSK-3β и в допълнение увеличава целите на каноничния път на иРНК Wnt/β-катенин в хипокампуса. Наскоро невроните, диференцирани от индуцирани плурипотентни стволови клетки на пациенти с шизофрения, показаха променена експресия на много компоненти по този път, включително различни изоформи на TCF/LF. 42 Освен това няколко открития при животни свързват няколко стъпки в тази каскада с депресивен и антидепресант, предизвикан от стреса отговор. 43 Участие на TCF/LF в невропсихиатрични разстройства и T2D го прави реален кандидат за сложен споделен генетичен риск.
В нашия анализ вариантът rs1625975 в CDH23, който е част от суперсемейството на кадхерините на гликопротеините на клетъчна адхезия, беше високо оценен. Доказано е, че няколко кадхерина потискат активността на β-катенина 44 и поради това се регулират отрицателно от Wnt сигнализиране. Няколко гена, кодиращи кадхерин и адхезивен гликопротеин, са свързани с BD в генетични изследвания. 46, 47, 48, 49, 50
Rs11150078 в WWOX представлява обратна връзка с връзката, наблюдавана с TCF7L2, което предполага защитен ефект на по-малкия алел върху риска от BD при увеличаване на ИТМ. Генът WWOX кодира протеин, който секретира транскрипционни фактори, участващи в новообразувания, 51 и дефектите са широко изследвани в раковата литература. WWOX взаимодейства с много сигнални пътища, включително Wnt, 52 г., но доколкото ни е известно, преди това не е било свързано с психиатрични разстройства.
Анализът на IPA мрежата определи интерактом, който свързва два от най-добрите ни гени, TCF7L2 и WWOX, заедно и подчерта други гени с потенциална значимост чрез взаимодействие с β-катениновите промотори Jun и Rap1 и инхибитора GSK-3β: сигнални каскадни молекули Akt надолу по веригата и Erk (Фигура 2). В допълнение, обогатената мрежа "клетъчна смърт и оцеляване" включва BD CACNA1C, 6 CACNA2D1 и CACNB3 рискови гени .
Това проучване включва допълнителна информация за макс. ИТМ за анализ на генома на риска от BD в целия геном и идентифициране на нови генетични варианти с биологично значение. Интересното е, че наблюдавахме генетични асоциации с по-голяма статистическа значимост от оригиналните анализи, въпреки факта, че нашите анализи бяха ограничени до тези, които имаха максимални данни за ИТМ (т.е. 388 случая/1020 контроли срещу 1001 случая/1034 контроли).). Тези резултати предполагат, че сме постигнали по-голяма мощност за откриване на генетични ефекти чрез намаляване на хетерогенността поради интеграцията на ключовия ковариант. Като цяло, най-високо оценените SNP в нашите анализи са доста различни от тези, докладвани от европейски американци в Smith et al. 4 Много от прогнозните коефициенти на вероятност за докладвани преди това най-добри SNP са отслабени в нашите анализи, което предполага, че ИТМ може да е объркващ фактор (Таблица 3). Въпреки това, rs7690204 в GYPA е високо оценен и в двете проучвания. Всъщност както rs7690204, така и rs10193871 в NCKAP5 (известен още като NAP5) показват по-силни защитни ефекти в нашите ИТМ анализи (Таблица 3).
Маса в пълен размер
Важно е да се осъзнае, че ИТМ може да бъде по-посредническа мярка, свързана с други основни състояния. Например, много от най-ефективните лекарства за лечение на BD, като невролептици, са свързани с увеличаване на теглото. Нашите анализи не вземат предвид настоящото лечение, което всеки отделен случай получава, нито наддаването на тегло, което може да е било свързано с това лечение, и следователно нашите резултати могат да бъдат объркани с вида на лекарството или отговора на лечението. Въпреки че е налична основна информация за доживотна употреба на антипсихотици, не е налична подробна информация за едновременната употреба на лекарства, продължителността и дозировката, отговора на лечението и свързаното с това наддаване; рядко е налице такава надеждна информация при ретроспективно проучване, което прави предизвикателство объркващите ефекти като лекарства или отговор на лечението. Изследването на въздействието на употребата на наркотици и свързаното с лечението наддаване на тегло върху наблюдаваните връзки е важна област за бъдещи изследвания.
Освен това в това проучване не разполагахме с данни за историята на T2D и следователно не можахме да проучим дали ИТМ може да замести предразположението към T2D. В допълнение към T2D, високият ИТМ е силно свързан с много заболявания и разстройства, включително други психиатрични разстройства и съпътстващи заболявания (като хранителни разстройства), както и метаболитни разстройства и сърдечни заболявания, което допълнително усложнява интерпретацията на нашите резултати. Идентифицирането на генетични фактори, корелирани с BD и BMI, е само началото на разбирането за причинно-следствените биологични и генетични механизми. Всъщност това проучване предполага потенциал за често срещани генетични рискови фактори между психиатрични черти и метаболитни нарушения, като BD и T2D, които значително се припокриват в предишни мрежови анализи. 7 Въпреки че не е пряко изследвано тук, настоящото изследване на често срещаните генетични рискови фактори за множество съпътстващи заболявания - плейотропни ефекти - може да хвърли светлина върху значимостта на констатациите от това проучване. Необходими са последващи кохортни и функционални проучвания, за да се разграничи сложността на тези връзки и да се разбере връзката между ИТМ и генетичното предразположение към BD.
Доколкото ни е известно, това проучване е първото, което едновременно изследва генетични рискови фактори за BD и затлъстяване в целия геном. В това проучване идентифицирахме много биологично значими генетични варианти, които са свързани с BD, като взехме предвид ефекта от максималния ИТМ. Необходимо е по-нататъшно проучване, за да се възпроизведат и валидират тези взаимоотношения и да се определи дали идентифицираните варианти или гени имат функционална роля в чувствителността към болести. За да се разбере по-добре генетичната етиология на BD и затлъстяването, е необходимо да се изследват сложни генетични връзки, включващи ковариати и генетични взаимодействия.
- Депресивното разстройство облекчава ефекта на гена fto върху индекса на телесна маса на молекулярната психиатрия
- Трябва да ядете броколи заради противораковия му ефект
- CPPPaP - Специфични затруднения в ученето - Дискалкулия
- Деца и разстройства sp; nku; като техен специален; подагра без лекарства; Мозък и нерви; Глава; На децата; заболявания
- Децата трябва да спят в креватчета най-малко три години, се казва в изследването