елементи
абстрактно
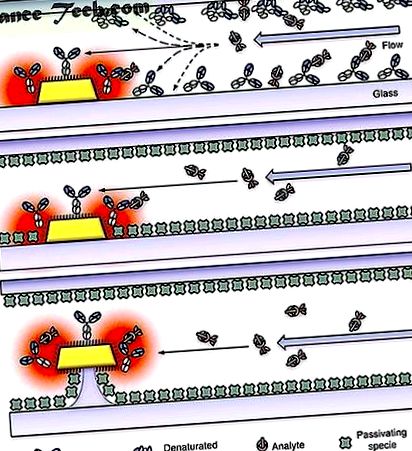
Наноплазмонично молекулярно сканиране в микрофлуидни канали. ( а ) Неспецифичното свързване ще изчерпи както рецепторната, така и целевата молекулна концентрация, ако каналът не е пасивиран, което води до забавена реакция на сензора и висока консумация на рецептор и цел. Стрелките представят възможните пътища на взаимодействие на молекулите на аналита. ( б ) Пасивирането на каналните повърхности от подходящи блокиращи видове намалява неспецифичното свързване, но блокиращите молекули заемат голяма част от най-чувствителния обем на плазмонното откриване. ( ° С ) Чрез увеличаване на металната частица върху оптимизираната нанопилария, плазмоничните полета се отделят от субстрата и пасивиращите молекули. Тази конфигурация значително увеличава ефективния обем на сканиране и подобрява общата производителност на сензора.
Изображение в пълен размер
Материали и методи
Производство на сензорни основи
Стъклените стъкла (24 х 24 mm # 5) се пречистват чрез обработка с ултразвук в ацетон и изопропанол в продължение на 5 минути и след това се покриват с титан (1 nm) и злато (50 nm) чрез пръскане чрез пулверизиране, както е показано на Фигура 2а. След това субстратите бяха обработени за кратко в кислородна плазма преди отливането на положително заредения PDDA (полидиалилдиметиламониев хлорид, 0,2 обемни% във вода, Sigma-Aldrich), както е показано на фиг. 2б. След кратко изплакване с вода, върху субстратите се излива разтвор от зърна с отрицателно заредена полистирол (PS) (0,1% във вода, Microparticles GmbH, Германия) (Фигура 2в). В зависимост от приложението, или PS мъниста са отстранени от половината от повърхността на субстрата с помощта на кубична лента, или субстратите са моделирани чрез PDMS микроконтактен печат (Фигура 2г). Самосглобените PS мъниста действаха като маска по време на последващото фрезоване на йонни лъчи (Ionfab 300, Oxford Instruments, UK; Фигура 2д). След това PS мъниста бяха отстранени с куб и субстратите бяха третирани в кислородна плазма за отстраняване на остатъчни PDDA фрагменти (Фигура 2f).
Осъществяване на нанопространства с нано-стълбове. Етапите в производствения процес са както следва:( а ) пръскане на материала; ( б ) отливане на положително зареден полимерен филм; ( ° С ) самостоятелно сглобяване на отрицателно заредени полистиролови (PS) мъниста; д ) микроизображение по избор с използване на PDMS печат; д ) смилане на йонни лъчи; ( е ) премахване на останалите PS мъниста чрез оголване на лентата; ( ж ) ецване на стъкления субстрат в BOE; з ) окончателен микроскоп със златни нанодискове върху стъклени нанопилари.
Изображение в пълен размер
Производство на PDMS структури
Формата за микроконтактен печат е направена чрез лазерна литография върху силициева плоча (mrDWL 5-отрицателен фоторезист, Allresist GmbH, Германия). Параметрите на процеса бяха настроени в съответствие с препоръките на производителя. Безмехурчената PDMS смес (10: 1, комплект Sylgard 184, Dow Corning, САЩ) се нанася върху формата при 250 rpm. След като се държи на тъмно за
40 часа, този процес доведе до окончателна дебелина на PDMS. 0,75–1 мм. Лепливата PDMS мембрана беше внимателно отлепена, преобърната върху златен субстрат, покрит с PS, където беше държана в контакт за 10 до 20 секунди и след това отстранена с едно непрекъснато движение. Подробно описание на метода за производство на микрофлуидни PDMS може да се намери на други места 31, 32 .
Оптична спектроскопия
Средните спектри на екстинкция са записани на UV-VIS-NIR спектрофотометър (Cary 2000, Agilent Technologies, USA). Наблюдението в реално време на дължината на вълната LSPR на отделни сканиращи петна беше извършено с помощта на модул за изчезване на дома, базиран на колимиран влакнесто-свързан източник на светлина (HL-2000, Ocean Optics, Dunedin, USA) и свързан с влакна спектрометър (BRC711E, B&W Tek, САЩ). Извършени бяха едновременни измервания на множество сканиращи петна с помощта на хиперспектрално устройство за изображения 33, 34, изградено около обърнат микроскоп (Eclipse Ti-E, Nikon, Япония), регулируем филтър от течни кристали (LCTF, спектрален диапазон 650 до 1100 nm, 7 честотна лента, Резолюция 1 nm, модел Varispec SNIR, PerkinElmer, САЩ) и CMOS камера (Neo5, Andor Technologies, Великобритания). Нашата система е специално проектирана за паралелно изследване в реално време и анализ в движение на множество места за сканиране чрез синхронизиране и контрол на всички основни оптични компоненти с помощта на персонализиран код Labview.
Електродинамични симулации
Оптичните симулации на симулациите на разпределение в близост до полето бяха извършени, като се използва търговска реализация на времево-диференциалната времева област (FDTD) (Lumerical, Inc., Канада) с оптични константи за злато на базата на 35 и формулировка на общо поле/разпръснато поле. D = 172, 200 или 280 nm, дебелина t = 60 nm, кривина на горния и долния ръб с радиус 5 nm и страничен ъгъл на конус от 20 °. RI на подложката/опората на стълба беше зададена на n = 1.52 и конструкциите бяха заобиколени от вода (n = 1.33). Размерът на окото е 4 nm, но е настроен на 0,5 nm около дисковете и гравираните профили.
Повърхностна химия
Първо, 0,1 mM SH-PEG-метокси (5 kDa, Rapp Polymere, Германия) се разтваря в етанол при 50 ° С. Субстратите се потапят в PEG разтвор за една нощ и след това се прикрепват към микрофлуидните структури на PDMS чрез нискотемпературно термично свързване ( 40 ° C) за 2 до 3 часа. Анти-PEG имуноглобулините Gs (IgG) E11 и E6.3 се поглъщат в 50% глицерол при концентрация 400 μg ml-1 (справка 36). Неутравидин (NTV; ThermoFischer Scientific) се разтваря в подходящия буфер (и) до концентрация 50 μg ml-1 и се използва като такъв.
Резултати и дискусия
Използвахме утвърден, евтин и мащабируем метод на колоидна литография 37, за да създадем добре дефинирани модели на нанодиск от късо разстояние на стандартни стъклени микроскопски стъкла. Съответните производствени стъпки са схематично показани на Фигура 2а - 2е, където също включихме незадължителна стъпка (Фигура 2г) на двуизмерно микро-вземане на проби, базирана на метода без асансьор, разработен от Andersson et al. 38. Този производствен протокол предоставя проби, напълно съвместими с микрофлуидни устройства и тестови протоколи, разработени преди това от Aćimović et al. 32. Контрастът между областите на наночастици и не наночастици, получени по този метод, е отличен, както е показано на допълнителната фигура.
Нанодисковите субстрати представляват началната точка за мокро офорт (Фигура 2g) за образуване на нанодискове върху тесни колони, както се съобщава от Otte et al. 29. Използваме стандартно буферирано оксидно офортване (BOE, 15% флуороводородна киселина). След внимателно изплакване с вода за спиране на процеса на ецване, пробите се изсушават под струя азот. Повърхностното напрежение, което е резултат от отстъпването на тънкия воден слой по време на сушене, може да доведе до счупване на нанопилповете и този ефект задава граница колко тънък може да бъде нанопилърът, което от своя страна ограничава минималния диаметър на нанодиска, необходим за постигане на разделяне на ЕМ. Поради тази причина се съсредоточихме върху златни нанодискове с по-голям диаметър, d, отколкото преди изследвахме 29 .
Фигура 3 обобщава морфологичните промени спрямо времето на ецване за три различни Au нанодискови проби с d = 170–290 nm. Предположихме, че скоростта на офорт може да бъде анизотропна поради триизмерен наноструктуриран пейзаж. За да тестваме тази възможност, първо определихме скоростта на вертикално ецване чрез сканиране с профилометър през границите с d = 290 nm нанодискове. Както може да се види на фигура 3а, тези данни са в отлично съответствие с известната номинална скорост на ецване на стъкло в BOE в нашата лаборатория (
90 nm min-1). След това изобразихме субстратите с помощта на сканиращ електронен микроскоп (SEM) под ъгъл на наклон 70 °, за да изчислим дълбочината на странично ецване директно под нанодисковете, получена като (d - d ′)/2, където d ′ е диаметърът на най-близкия до нанодиска нанопилър. Данните на фигура 3а показват скорост на странично ецване от 77,5 nm min-1 (линейно прилягане), демонстрираща значителна, но благоприятна анизотропия на ецване, вероятно поради дифузионна нехомогенност. И накрая, въз основа на SEM анализ на изображението, ние оценихме минималния механично стабилен диаметър на нанопилър при d be50 nm. Фигура 3b сравнява не гравирани дискове (вляво) и дискове, поддържани от нанопилари d = 50 nm (вдясно).
Създаване на нанопилари под златни нанодискове чрез офорт в BOE. а ) Вертикални (червени точки) и странични (черни точки) дълбочини на ецване на стъкло за основи, покрити със златни нанодискове с различен диаметър d. Номинална скорост на ецване прибл. 90 nm min-1 е обозначена с пунктирана линия. Лентите за грешки представляват стандартното отклонение на наборите данни. ( б ) SEM изображения под ъгъл на наклон от 70 ° на представителни популации от немодифицирани и гравирани златни нанодискове с различен диаметър d (скала на скалата = 100 nm).
Изображение в пълен размер
Изображение в пълен размер
Извършихме електродинамични изчисления, използвайки метода FDTD, за да обосновем нашето твърдение пред EM отдела и да разберем по-добре оптималните параметри на структурата. Изчислихме оптичната реакция за отделни нанодискове с диаметър d = 172, 200 и 280 nm, които напълно съответстват на експерименталните стойности, но приехме изотропна динамика на ецване, за да съкратим времето за изчисление и усилията за моделиране. Както е обобщено на Фигура 4в, изчислените пикови позиции показват подобна експоненциална тенденция като тенденцията, наблюдавана в експериментите. Широчината на линията LSPR също показва експоненциално разпадане (Фигура 4в, вмъкване), въпреки че експериментите показват само общо намаляване на пълната ширина до половината от максимума, вероятно поради нехомогенно разширяване, например от размера на полидисперсността на PS мъниста (Фигура 4c 4б, вмъкване). Изчисленията показват, че резонансните плата не са напълно равни, отчасти поради предполагаемото изотропно, а не анизотропно офортване, но имат много ниски наклони във времето. Проверихме извеждането на резонансното положение като функция от дълбочината на ецване, за да определим най-високата степен на отделяне на ЕМ, постижима за избрания минимален нанопиларен диаметър d = 50 nm (Фигура 4d). Данните показват, че минималната абсолютна стойност,
0, 12 nm на nm дебелина на адсорбирания слой се получава за 200 nm дискове. Първоначалните производни, при нулева дълбочина на офорт, представляват реакцията на дисковете към безкрайно тънък слой с RI = 1,52, образуван върху стъклото. За 200 nm диск тази стойност е
40 пъти стойността на производната за същия диск, поддържана от колоната d = 50 nm. По този начин нанодискът е по същество отделен от основата за оптимално гравирана структура. Фигура 4д илюстрира съответните промени в интензивността на ЕМ в близко поле при резонанс за тези два ограничаващи случая, показващи значително намаляване на пространственото припокриване между субстрата и субстрата за нанодиска, поддържан от колона.
За да демонстрираме предимството на отделянето на ЕМ за приложения на биосензори, решихме да работим с проста система от модели, напомняща на идеална стратегия за тестване, както е показано на фигури 1б и 1в. Използваме NTV като пасивиращ обект поради почти необратимата му адсорбция върху стъкло при неутрално рН 40. Рецепторът е 5 kDa тиол-ПЕГ-метокси, който се свързва изключително със златото и ефективно отблъсква протеини 41, като по този начин отговаря на изискването за ниско кръстосано замърсяване между пасивиращите видове и рецепторния биорекогенен слой. Първо изследвахме LSPR отговора на покритите с ПЕГ нанодискове към NTV (50 μg ml-1), поради което се очаква да се свързва почти изключително със стъкления субстрат. Фигура 5а обобщава реакцията след инжектиране на NTV с 210 nm дискове, изложени на офорт 0, 10, 30 и 50 s в BOE. За най-дългото време за ецване, което е значително по-кратко от 65 s, границата за 210 nm дискове, откликът намалява с около порядък в сравнение с неприкрепения случай (вж. Вмъкване на фигура 5а за абсолютното върхово отместване). стойности).
Изображение в пълен размер
25%. По този начин можем да заключим, че всички основни сензорни характеристики на нанодисковите LSPR сензори са подобрени чрез EM отделяне, както е обобщено във вмъкването на Фигура 5b.
Съвместимост на дискове, поддържани от стълбове, с процеса на кръстосано подравняване и сливане в PDMS микрофлуиден интерфейс в голям мащаб. а ) Част от устройството, където 64 лъскави квадрата (в проходите между каналите и плазмоничния субстрат на микропатията) представляват 64 сканиращи точки. Тези места бяха използвани за проверка на времето за вземане на проби и независимостта от шума на броя на местата за сканиране (данните не са показани). Вложката показва устройството (24 × 24 × 5 мм) до монетата (1 SEK). ( б ) Сензограма в реално време, сравняваща взаимодействието на два вида анти-PEG IgG като функция от концентрацията на антитела.
Изображение в пълен размер
заключения
- Вкусна закваска, сладкиши, рецепта
- Отлични зелеви котлети - идеална храна по време на карантина Имате нужда само от 4 основни съставки и
- Отлични кюфтета в доматен сос, топ РЕЦЕПТА Добра кухня
- Вкусни сирена безглутенови ньоки за сладко със сос от смокини - Fitshaker
- Отлични свойства на медното всемогъщество при болести и средство за запазване на доброто и здравословно живеене